Produktinformation
Pharmazeutischer Standard
VESOXX® ist ein industrielles Fertigarzneimittel für die intravesikale Therapie der neurogenen Detrusorüberaktivität. Im Rahmen eines dezentralen Zulassungsverfahrens wurde der Nachweis der Wirksamkeit, Unbedenklichkeit und angemessenen pharmazeutischen Qualität erbracht.
VESOXX® (1mg/ml Oxybutynin-HCI) wird angewendet zur Unterdrückung einer neurogenen Detrusorüberaktivität (Neurogenic Detrusor Overactivity; NDO) bei Kindern ab 6 Jahren und bei Erwachsenen, die ihre Blase mittels sauberer intermittierender Katheterisierung (CIC) entleeren, wenn sie durch eine Behandlung mit oralen Anticholinergika aufgrund mangelnder Wirksamkeit und/oder unerträglicher Nebenwirkungen nicht adäquat eingestellt werden können.1

VESOXX® als 2. Linientherapieoption
Bei der intravesikalen Therapie mit VESOXX® (1 mg/ml Oxybutynin-HCl) werden eine hohe, lokale Konzentration in der Blase und ein schneller Wirkeintritt erreicht.
Auf Basis von urodynamischen Parametern wird die Tagesdosis patientenindividuell bestimmt. Durch die Instillation des Wirkstoffs unmittelbar in die Blase wird ein Einsatz direkt am Wirkort ermöglicht. Die direkten Wirkungen von VESOXX® in der Blase und der geringe First-Pass-Metabolismus lassen eine hohe Effektivität und eine bessere Verträglichkeit im Vergleich zur oralen Therapie erwarten.1-6
Instillation nach Katheterisierung
VESOXX® ist eine klare, farblose Lösung aus 0,1 % Oxybutynin-Hydrochlorid (1 mg/ml).1
VESOXX® (1 mg/ml Oxybutynin-HCl) wird nach der intermittierenden Katheterisierung ein- bis mehrmals täglich in die Blase instilliert und kann nahtlos in den Alltag integriert werden.1

- VESOXX® Fachinformation.
- Humblet M. et al., Long-term outcome of intravesical oxybutynin in children with detrusor-sphincter dyssynergia: with special reference to age dependent parameters. Neurourol Urodyn. 2015; 34(4):336–342. (retrospektive Kohortenstudie mit intravesikalem Oxybutynin, n = 10 bei Re-Evaluation).
- Krause P. et al., Pharmacokinetics of intravesical versus oral oxybutynin in healthy adults: results of an open-label, randomised, prospective clinical study. J Urol. 2013; 190(5):1791–1797; (prospektive, randomisierte Cross-Over Open-Label-Studie (Periode I und II: orales oder intravesikales Oxybutynin, Periode III: intravesikales Oxybutynin), n = 20).
- Buyse G. et al., Intravesical Oxybutynin for neurogenic bladder dysfunction: less systemic side effects due to reduced first pass metabolism. J Urol. 1998; 160(3 Pt 1):892–896; (Vergleichsstudie mit intravesikalem (n = 11) und oralem Oxybutynin (n = 5)).
- Oki T. et al., Demonstration of bladder selective muscarinic receptor binding by intravesical oxybutynin to treat overactive bladder. J Urol, 2004. 172(5 Pt 1): p. 2059-64; (präklinische Studie an Ratten mit oralem und intravesikalem Oxybutynin).
- Schröder A. et al., Efficacy, Safety, and Tolerability of Intravesically Administered 0.1 % Oxybutynin Hydrochloride Solution in Adult Patients With Neurogenic Bladder: A Randomized, Prospective, Controlled Multi-Center Trial. Neurourol Urodyn. 2016; 35(5):582–588; (randomisierte, prospektive, aktiv kontrollierte, multizentrische Open-Label-Studie mit intravesikalem Oxybutynin (n = 18) und oralem Oxybutynin (n = 17)).
Der multimodale Wirkmechanismus
von intravesikalem Oxybutynin wie VESOXX®
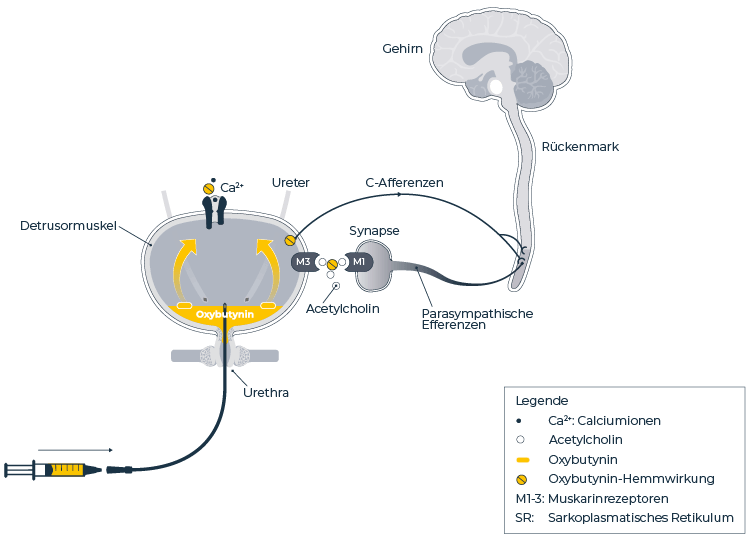
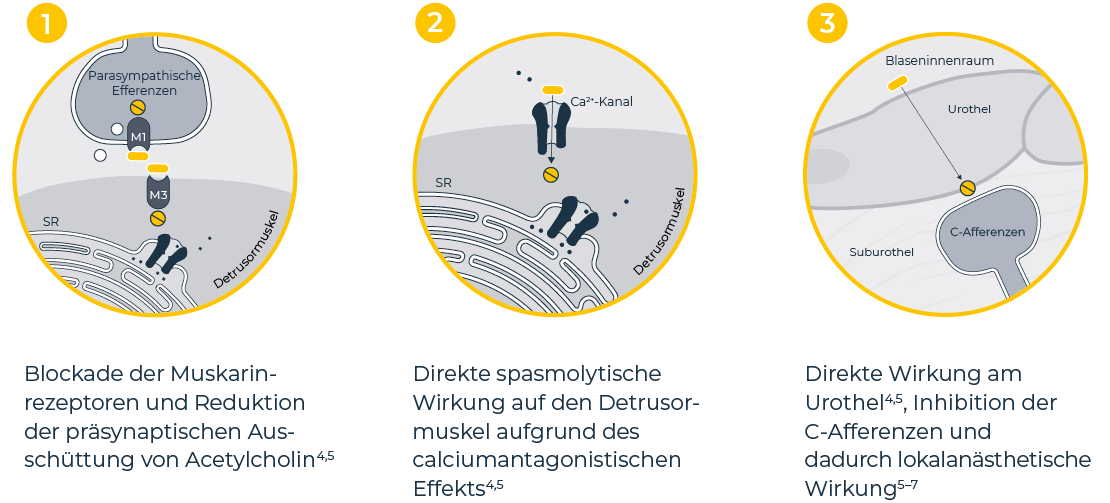
Erstellt nach Murakami S. et al. 2003, Chapple C.R. et al. 2002, Kim Y. et al.
2005 und De Wachter S. et al. 2003.4-7
- Ford A.P.D.W. et al., Purinoceptors as therapeutic targets for lower urinary tract dysfunction. Br J Pharmacol. 2006; 147(Suppl 2):132–143; (Übersichtsartikel).
- Fowler C.J. et al., The neural control of micturition. Nat Rev Neurosci. 2008; 9(6):453–466; (Übersichtsartikel).
- Giglio D. and Tobin G., Muscarinic Receptor Subtypes in the Lower Urinary Tract. Pharmacology. 2009; 83(5):259–269; (Übersichtsartikel).
- Murakami S. et al., Pharmacological Effects of KRP-197 on the Human Isolated Urinary Bladder. Urol Int 2003; 71(3):290-298; (präklinische Studie an isoliertem humanen Blasengewebe mit Antimuskarinika).
- Chapple C.R., Yamanishi T. and Chess-Williams R., Muscarinic receptor subtypes and management of the overactive bladder. Urology, 2002. 60 (5 Suppl 1): p. 82-8; discussion 88-9; (Übersichtsartikel).
- Kim Y. et al., Antimuscarinic agents exhibit local inhibitory effects on muscarinic receptors in bladder-afferent pathways. Urology, 2005. 65(2): p. 238-42; (präklinische Studie an Ratten mit intravesikalen Antimuskarinika).
- De Wachter S. and Wyndaele J.J., Intravesical oxybutynin: a local anesthetic effect on bladder C afferents. J Urol, 2003. 169(5): p. 1892-5; (präklinische Studie an Ratten mit intravesikalem Oxybutynin).
Verordnung
VESOXX® in allen Apotheken erhältlich

VESOXX® (1 mg/ml Oxybutynin-HCl) ist in allen Apotheken als 100×10-ml-Fertigspritzen erhältlich.
Lagerung: Keine Kühlung erforderlich, kann bei Raumtemperatur gelagert werden
Haltbarkeit: 36 Monate
PZN: 16941443
Erstattung durch Krankenkassen


IndividuellePraxisbesonderheit
Unterscheidet sich Ihre Praxis erheblich vom Durchschnitt – weil sie etwa außergewöhnlich behandlungsaufwändige Patient*innen mit VESOXX® therapieren – können Sie diese kostenintensiven Einzelfälle bei den Krankenkassen geltend machen. Nutzen Sie hierfür unser Factsheet.
VESOXX® Fachinformation.
